На протяжении десятилетий идиопатическая внутричерепная гипертензия (ИВГ) – также известная как псевдоопухоль мозга или, в русскоязычной литературе, доброкачественная внутричерепная гипертензия – носит название, по сути сообщающее пациенту, что причина заболевания неизвестна. Состояние определяется как повышение давления спинномозговой жидкости (ликвора) при отсутствии опухоли мозга, гидроцефалии и других очевидных структурных причин 1 Пациенты, как правило, страдают ожирением, относятся к женскому полу и находятся в репродуктивном возрасте 2 3 Они обращаются с инвалидизирующими головными болями, пульсирующим шумом в ушах, застойным диском зрительного нерва, преходящим затуманиванием зрения и прогрессирующей потерей зрения 4
В классическом нарративе ответственность возлагается на ожирение, гормональные факторы и расплывчатые нарушения реабсорбции ликвора. Однако на практике этот нарратив оставляет многих пациентов без ответа и без эффективного долгосрочного лечения. Растущий объём данных показывает, что у значительной части пациентов повышенное давление вовсе не идиопатическое – это результат механической обструкции венозного оттока от головного мозга 5 6 7
Две из наиболее недооценённых обструкций возникают в очень специфических анатомических узких местах: внутренней яремной вены на уровне первого шейного позвонка (C1) и подключично-плечеголовного венозного коридора в области грудного выхода. Оба эти участка должны быть в дифференциальном диагнозе у каждого пациента с диагнозом ИВГ – особенно у тех, чьи симптомы сохраняются несмотря на снижение веса, приём ацетазоламида, люмбальные пункции, ликворные шунты и даже стентирование венозных синусов.
В этой статье разбираются обоснование, анатомия, доказательная база и практические следствия такого подхода.
Что такое ИВГ – краткое напоминание
Действующий диагностический стандарт – критерии Фридмана 2013 года, требующие 1
- Симптомы и признаки генерализованной внутричерепной гипертензии или застойного диска зрительного нерва
- Нормальный неврологический осмотр, за исключением нарушений со стороны черепных нервов
- Нормальные результаты нейровизуализации (отсутствие объёмного образования, гидроцефалии или структурного поражения)
- Нормальный состав ликвора
- Повышенное начальное давление при люмбальной пункции (>25 см H₂O у взрослых, >28 см H₂O у детей)
Если выявляется любая причина – тромбоз дуральных синусов, приём определённых препаратов, эндокринное заболевание – случай реклассифицируется как вторичная внутричерепная гипертензия, и метка «идиопатическая» снимается. Проблема в том, что в рамках действующей парадигмы клиницисты редко ищут венозную обструкцию за пределами черепа. Стандартная визуализация останавливается на основании черепа, пациент во время сканирования лежит на спине с прямо поставленной головой, а динамические сужения, проявляющиеся только в вертикальном положении или при повороте головы, остаются невидимыми.
В результате пациент с прекрасно идентифицируемой механической причиной получает диагноз идиопатической формы и лечится симптоматически.
Классическая демография остаётся в силе – но не объясняет всю картину
- ИВГ встречается у женщин примерно в 9 раз чаще, чем у мужчин 3
- Пик заболеваемости приходится на возраст 20–40 лет 3
- Самым сильным классически признанным фактором риска остаётся ожирение, имеющееся у 70–94% пациентов 2
- До 40% пациентов развивают стойкое нарушение зрения, а 1–10% становятся юридически слепыми 3
Эти цифры реальны, и ожирение действительно играет роль – повышенное внутрибрюшное и центральное венозное давление действительно повышают внутричерепное венозное давление 5 Но одно лишь ожирение не объясняет ни худощавого пациента с ИВГ, ни пациента с рефрактерным течением болезни на фоне снижения веса, ни пациента с идиопатической внутричерепной гипертензией без отёка диска зрительного нерва (IIHWOP) 8
Гипотеза яремной вены – объединяющая модель
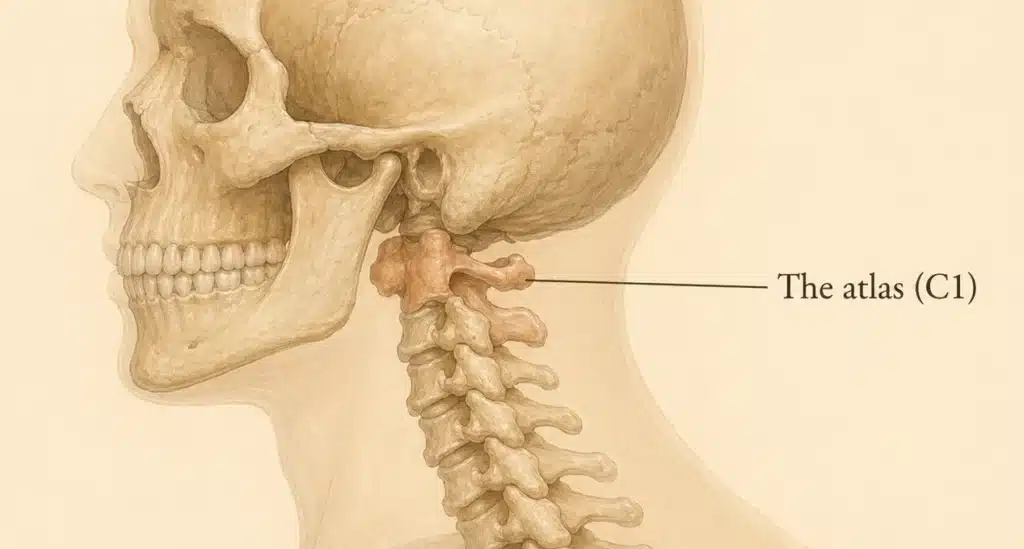
В 2024 году Fargen, Midtlien, Margraf и Hui опубликовали наиболее значимое в последнее время переосмысление патогенеза ИВГ – гипотезу яремной вены 5 Их центральный аргумент состоит в том, что ИВГ и расстройства её спектра лучше всего понимать как проблему венозного оттока от головного мозга, в которой внутренние яремные вены (ВЯВ) играют главную, уязвимую и часто упускаемую из виду роль.
Их модель сводится к шести положениям 5
- Внутренние яремные вены подвержены физиологической и патологической компрессии на всём протяжении – на уровне C1 шиловидным отростком, а между C3 и C6 – динамическими мышечными и каротидными воздействиями.
- Выраженный динамический стеноз ВЯВ с большими градиентами давления на шейном уровне распространён у пациентов спектра ИВГ и существенно влияет на внутричерепное венозное давление и давление ликвора.
- Внеяремные коллатеральные пути со временем расширяются, но они недостаточны для замены нормального оттока через яремные вены.
- Плохой отток через ВЯВ приводит к внутричерепной венозной гипертензии и застою, повышая давление ликвора и внутричерепное давление (ВЧД).
- Глимфатическая система также испытывает застой, но не способна компенсировать.
- Стойко повышенное ВЧД со временем приводит к экстрамуральной компрессии поперечного синуса – той самой классической находке на визуализации, которая выступает усилителем процесса, а не его первопричиной.
Последний пункт принципиален и регулярно неправильно интерпретируется в клинической практике. Стеноз поперечного синуса на МР-венографии – это находка, доминирующая в обследованиях при ИВГ на протяжении двух десятилетий, тогда как гораздо более проксимальная – и физиологически более значимая – обструкция на уровне внутренней яремной вены практически не попадает в заключение по визуализации. Клиническое внимание сосредоточено на следствии вниз по течению, а не на причине вверх по течению. Вопрос «что первично – курица или яйцо» был впервые формально поставлен Корбеттом и Дигре в 2002 году 9 и с тех пор ответ стал достаточно ясен. Кинг и соавторы в том же году показали, что снижение давления ликвора путём латеральной C1 – C2-пункции немедленно устраняет повышенное давление в венозных синусах, измеренное при прямой манометрии 10– наблюдение, принципиально несовместимое с тем, чтобы стеноз был первопричиной выше по течению. Последующие исследования визуализации многократно подтверждали ту же картину: стенозы поперечных синусов разрешаются при катетерной и КТ-венографии – порой в течение часа – после удаления ликвора или шунтирования 11
Объективности ради – обратимость не универсальна. Боно и соавторы наблюдали четырнадцать пациентов с ИВГ и двусторонним стенозом поперечного синуса по серии МР-венографий в течение шести лет и обнаружили, что стенозы сохранялись даже у тех девяти пациентов (64%), у которых давление ликвора нормализовалось на медикаментозной терапии 12– что свидетельствует о том, что в части случаев синус подвергается структурной перестройке, перестающей реагировать на одно лишь снижение ВЧД. Де Симоне и соавторы синтезировали эти противоречивые наблюдения в модель замкнутого контура самоограничивающегося венозного коллапса: исходное повышение давления ликвора сдавливает податливый сегмент синуса, возникающее повышение венозного давления далее снижает реабсорбцию ликвора, и оба давления стабилизируются на новом, более высоком равновесном уровне 13 Эта модель объясняет обе картины: у одних пациентов контур прерывается острым удалением ликвора, и стеноз обращается; у других, особенно при длительном течении болезни, равновесие закрепляется, и стеноз сохраняется несмотря на нормализацию давления. В любом случае стеноз поперечного синуса – самоусиливающийся участник процесса, а не его исходная причина.
Именно поэтому значительная часть пациентов даёт рецидив после стентирования венозных синусов. Систематический обзор и мета-анализ 2024 года 694 пациентов с ИВГ из 24 исследований сообщил о суммарной частоте рестеноза 17,7% и о 22,3% пациентов с сохраняющимися или ухудшившимися симптомами после стентирования; авторы заключили, что эти показатели подчёркивают необходимость дальнейшего изучения процедуры 14 Более раннее когортное исследование Ахмеда и соавторов проследило 52 пациентов с ИВГ после стентирования поперечного синуса и сообщило, что у 6 пациентов (11,5%) развился рецидив симптомов, обусловленный одновременно повышенным венозным давлением и новым стенозом непосредственно рядом с исходным стентом, потребовавший повторной процедуры стентирования; одному пациенту в итоге понадобилось четыре 15 Стент расправляет следствие, тогда как обструкция выше по течению – на уровне яремной вены или ниже – остаётся полностью не затронутой 5
Точка компрессии №1: Стеноз внутренней яремной вены на уровне C1 (стилоидогенная компрессия яремной вены)
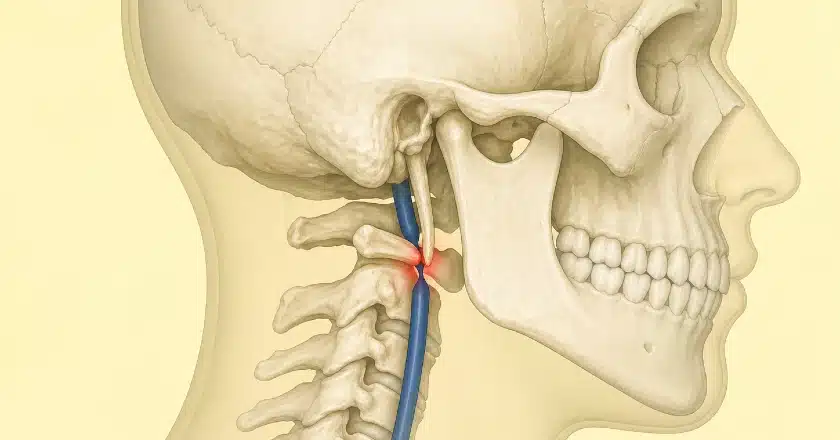
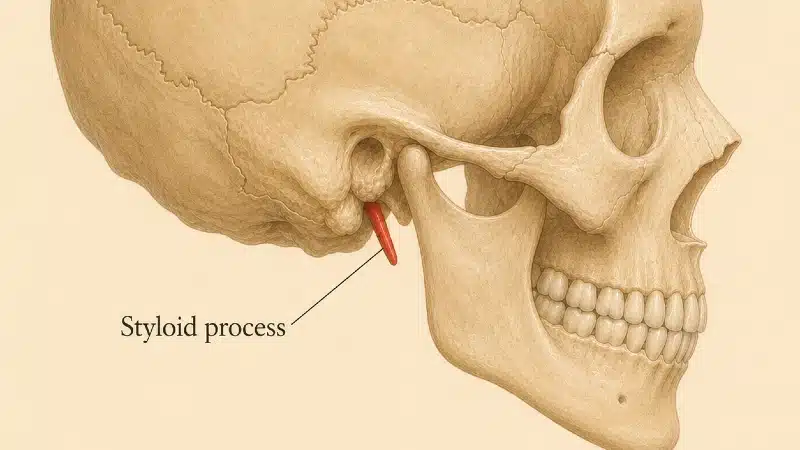
Внутренняя яремная вена покидает череп через яремное отверстие и сразу попадает в узкий коридор между двумя твёрдыми структурами: шиловидным отростком височной кости спереди и поперечным отростком первого шейного позвонка (C1, атланта) сзади. У некоторых людей этот коридор настолько узок, что вена оказывается механически зажата – это явление известно как синдром стилоидогенной компрессии яремной вены 16 17 18 19
Аналогия – садовый шланг, придавленный двумя камнями. Даже относительно нормальной длины шиловидный отросток способен вызывать выраженное сужение, если он направлен медиально или если поперечный отросток C1 необычно крупный либо расположен латерально 18 Мягкотканные участники процесса – двубрюшная мышца, затылочная артерия, проходящая петлёй вокруг вены, прямые мышцы головы, фиброзные тяжи внутри сонного влагалища – дополнительно усугубляют обструкцию 19
Почему компрессия на уровне C1 имеет значение для ИВГ
При компрессии ВЯВ на уровне C1 кровь застаивается в дуральных венозных синусах, и венозное давление в головном мозге растёт. Поскольку реабсорбция ликвора зависит от градиента давления между ликвором и кровью венозного синуса, составляющего примерно 3–5 мм рт. ст. 5 любое повышение венозного давления вынуждает компенсаторно расти и давление ликвора. У пациента развиваются головные боли, пульсирующий шум в ушах, отёк диска зрительного нерва, преходящее затуманивание зрения, мозговой туман – и ему ставится диагноз ИВГ.
Несколько исследовательских групп сейчас демонстрируют, что устранение яремной обструкции разрешает внутричерепную гипертензию у тщательно отобранных пациентов с нормализацией начального давления при люмбальной пункции и регрессом симптомов 20 Хирургическая декомпрессия – удаление шиловидного отростка, поперечного отростка C1 или того и другого с устранением мягкотканных компрессоров – представляет собой наиболее логичный и устойчивый подход, поскольку устраняет действительную механическую причину, а не расправляет вену против непреодолимого внешнего давления.
Признак, который большинство клиницистов упускают: позиционные симптомы
Компрессия ВЯВ на уровне C1 динамична – она усиливается при движениях шеи и при горизонтальном положении пациента (поскольку ВЯВ является доминирующим путём оттока от мозга в положении лёжа). Пациент, у которого головная боль сильнее всего при пробуждении, который инстинктивно спит полусидя, у которого шум в ушах исчезает при ручном надавливании на шею и который замечает мозговой туман после поворотов головы, описывает не признаки мигрени, а механические признаки.
Точка компрессии №2: Грудной выход – забытый уровень
Здесь начинается более интересная часть разговора, и здесь же литература лишь недавно начала наверстывать упущенное.
Внутренняя яремная вена впадает в сердце не напрямую. Она соединяется с подключичной веной позади медиального конца ключицы, образуя плечеголовную (безымянную) вену, которая затем пересекает верхнее средостение и впадает в верхнюю полую вену. Весь этот участок – от медиального конца ключицы до ВПВ – проходит через грудной выход, то самое анатомическое узкое место, в котором развивается синдром грудного выхода (синдром верхней апертуры грудной клетки).
Большинство клиницистов воспринимают синдром грудного выхода как проблему плечевого сплетения или подключичной артерии. Это стандартная парадигма, и в своих рамках она верна – нейрогенная форма составляет 80–85% случаев. Однако венозный компонент распространён шире, чем предполагают учебники, и его последствия выходят далеко за пределы руки.
Внеяремная венозная сеть
Внутренние яремные вены – доминирующий путь венозного оттока от мозга в положении лёжа. Однако в вертикальном положении ВЯВ оказываются выше уровня сердца и спадаются под атмосферным давлением, прекращая выполнять функцию основного канала оттока 21 В этой ситуации венозная кровь от мозга шунтируется в альтернативную систему – внеяремную венозную сеть (ВЯС, англ. EJN).
ВЯС включает позвоночное венозное сплетение (внутреннее и внешнее), глубокие шейные вены, наружную яремную вену и эмиссарные вены задней черепной ямки. На основании черепа эти два пути анатомически связаны через передний кондилярный синус (ПКС) Тролара – венозный узел в области наружного отверстия канала подъязычного нерва, соединяющий луковицу яремной вены непосредственно с позвоночным сплетением через мыщелковые вены 22 Математическое моделирование и визуализационные исследования в вертикальном положении показывают, что в положении стоя позвоночное сплетение становится доминирующим путём оттока венозной крови от мозга, тогда как ВЯВ несут меньшую долю 21 23 Обе системы функционируют как параллельные контуры, сходящиеся в одной анатомической точке окончания – в подключичных и плечеголовных венах у основания шеи.
Как синдром грудного выхода перегружает венозный отток от мозга
Именно схождение этих двух дренажных систем у основания шеи и связывает синдром грудного выхода с внутричерепным давлением. Когда подключичная вена хронически сдавлена в области рёберно-ключичного промежутка, кровь от верхней конечности не может вернуться через обструированный сегмент и направляется по коллатеральным путям.
Систематическая литература по визуализации точно документирует, куда уходят эти коллатерали. В обзоре грудных коллатеральных путей Marini и соавторов шейные венозные каналы определяются как первичная коллатеральная территория при обструкции подмышечной и подключичной вен 24 Названные передние шейные пути включают внутреннюю яремную вену, наружную яремную вену, яремную венозную дугу, нижнюю щитовидную вену и позвоночное венозное сплетение. Задние шейные коллатерали – описываемые как более частые и более выраженные – проходят через то же позвоночное сплетение и могут либо переходить на противоположную сторону, либо дренироваться в стенку грудной клетки и систему непарной вены 24
Эти коллатеральные каналы – те самые сосуды, из которых состоит внеяремная венозная сеть, дренирующая головной мозг. У пациента с венозной формой синдрома грудного выхода ВЯС, таким образом, выполняет одновременно две функции: дренирует верхнюю конечность через ретроградный коллатеральный кровоток и одновременно дренирует головной мозг. В горизонтальном положении ВЯВ открыты и обеспечивают основную часть венозного возврата от мозга, и эта двойная нагрузка может переноситься. В вертикальном положении, когда ВЯВ спадаются и мозг физиологически зависит от внеяремной сети, система оказывается перегруженной. Венозная кровь от мозга не может эффективно оттекать через каналы, уже заполненные ретроградным коллатеральным потоком от подключичной системы. Следствие – нарушение венозного оттока мозга, повышенное церебральное венозное давление и – через зависящий от давления механизм реабсорбции ликвора – повышенное внутричерепное давление.
Это перенаправление кровотока было непосредственно зафиксировано на изображениях. В 2017 году Chahwala и соавторы описали пациентку с инвалидизирующими мигренями, которым предшествовал односторонний отёк руки. На динамической венографии при приведении руки контраст, введённый в подключичную вену, потёк ретроградно в ипсилатеральную внутреннюю яремную вену, и обширные коллатеральные каналы перенаправляли кровь к голове 25 Её мигрени полностью разрешились после скаленэктомии и резекции первого ребра. Это наиболее прямая ангиографическая демонстрация в опубликованной литературе того, что рёберно-ключичная венозная обструкция способна перенаправлять венозный возврат от руки в путь оттока от мозга.
Высокая распространённость аномалий ВЯВ у пациентов с синдромом грудного выхода по данным рутинной венографии согласуется с этой физиологией. В проспективном венографическом исследовании последовательных пациентов с нейрогенной формой синдрома Ahn и соавторы выявили стеноз внутренней яремной вены у 76,2% (двусторонний – у 47,6%), наряду со стенозом подключичной вены у 82,5% 26 ВЯВ, рекрутированная как ретроградный коллатеральный путь для обструированной подключичной системы, вполне ожидаемо будет выглядеть суженной и окружённой аномальными коллатералями при контрастном исследовании – независимо от того, лежит ли в основе фиксированная компрессия или функциональный застой.
Сорок лет клинических данных – операция при синдроме грудного выхода уменьшает упорные головные боли
Аргумент о том, что синдром грудного выхода вносит вклад в повышенное внутричерепное давление, не нов. Ему сорок лет, но литература остаётся разбросанной по сосудистой хирургии, неврологии и нейроофтальмологии и до сих пор не сведена в общую концепцию.
В 1985 году Raskin, Howard и Ehrenfeld наблюдали тридцать последовательных пациентов с синдромом грудного выхода в течение как минимум шести месяцев после трансаксиллярной резекции первого ребра. У двадцати шести из тридцати пациентов рецидивирующая головная боль предшествовала появлению боли в шее и плече. После операции тринадцать пациентов полностью избавились от головной боли, одиннадцать ранее нетрудоспособных пациентов вернулись к работе, и ещё одиннадцать сообщили о появлении новой реакции на вазоактивные препараты, ранее неэффективные 27 На тот момент механизм объясняли расплывчатыми «сосудистыми факторами». Сегодня у нас есть значительно более чёткая ангиографическая картина того, как эти факторы выглядят, – что и продемонстрировал случай Chahwala 2017 года, описанный выше.
Наиболее свежая и крупная серия, опубликованная Cha и соавторами в 2025 году в журнале Clinical Anatomy, проанализировала пятьдесят последовательных пациентов с двойным диагнозом «хроническая мигрень и синдром грудного выхода» 28 Клинические особенности оказались показательными:
- Головные боли были строго односторонними или более выраженными на стороне поражения у 76% пациентов
- Сопутствующий отёк конечности отмечался у 67%
- 84% сообщили об усилении головной боли в положении лёжа – именно той картине, которую следует ожидать, когда внутричерепный отток во время сна всё больше зависит от яремного пути
Тридцати двум из пятидесяти пациентов была выполнена хирургическая декомпрессия с существенным улучшением выраженности головной боли 28 Усиление боли в горизонтальном положении – это прикроватный «отпечаток пальца» болезни нарушенного венозного оттока от мозга. Пациенты описывают пробуждение с головной болью, инстинктивный сон полусидя и то, что приподнятое положение головы приносит больше облегчения, чем медикаменты.
Совокупно факты складываются в единую согласованную историю, охватывающую сорок лет. Клиническое наблюдение Raskin 1985 года – разрешение головных болей после резекции первого ребра 27 Анатомическое подтверждение Ahn 2014 года – стеноз ВЯВ у 76% пациентов с нейрогенной формой синдрома 26 Ангиографическая демонстрация Chahwala 2017 года – ретроградный кровоток в систему венозного оттока от мозга при обструкции на уровне грудного выхода 25 Современная серия Cha 2025 года – документирование прикроватных признаков и хирургической отзывчивости у пятидесяти пациентов 28 Каждая из этих работ опубликована в специализированных журналах разных направлений, и до сих пор поле не выполнило их синтез. Этот синтез и есть то, что пытается сделать настоящая статья.
Сводя воедино: двухуровневая модель венозного оттока от мозга
Когда ИВГ рассматривается как нарушение венозного оттока, клиническая картина существенно проясняется. Венозная кровь от мозга должна последовательно преодолеть несколько узких мест:
- От дуральных синусов через яремное отверстие
- Мимо коридора «шиловидный отросток – C1» (точка компрессии 1)
- Через динамические мышечные и каротидные взаимоотношения на уровне C3 – C6
- Через рёберно-ключичное пространство грудного выхода (точка компрессии 2)
- Через плечеголовную вену и верхнюю полую вену в правое предсердие
Узкое место на любом из этих уровней повышает давление выше по течению, а узкие места на нескольких уровнях усугубляют проблему совокупно. Поскольку система динамична – на неё влияют положение головы, положение руки, дыхание и поза – стандартная статическая визуализация в положении лёжа регулярно упускает эти наслоившиеся обструкции.
Эта модель объясняет некоторые из наиболее обескураживающих наблюдений в практике лечения ИВГ:
- Почему процедуры отведения ликвора и медикаменты, снижающие его выработку, дают лишь временное облегчение – они не воздействуют на механическую обструкцию выше по течению
- Почему часть пациентов даёт рецидив после снижения веса (механическая обструкция не зависит от ИМТ)
- Почему «идиопатическая» внутричерепная гипертензия столь существенно перекрывается с фенотипами синдрома грудного выхода, синдрома Игла, СПОТ, синдрома Элерса – Данлоса и спонтанной ликвореи 29 30
- Почему отёк диска зрительного нерва может отсутствовать (форма IIHWOP), когда коллатерали частично компенсируют 8
Диагностические следствия – что нужно визуализировать
Если у пациента имеется фенотип ИВГ, обследование не должно ограничиваться МРТ головного мозга и люмбальной пункцией. Полная оценка венозного оттока должна включать:
- КТ-венографию (КТВ) головы и шеи – на сегодня золотой стандарт визуализации коридора «шиловидный отросток – C1» и количественной оценки яремного стеноза 16 17
- МР-венографию (МРВ) – полезна для оценки характера кровотока и состояния коллатералей 5
- Динамическую визуализацию – исследование в разных положениях головы и, при возможности, в вертикальном положении, поскольку статические снимки в положении лёжа недооценивают динамический стеноз 5
- Катетерную венографию с измерением давления – единственный надёжный способ количественно оценить транс-стенотические градиенты; градиенты >3–5 мм рт. ст. через стеноз клинически значимы 20
- Венографию плечеголовной и подключичной вен – особенно если у пациента есть какие-либо симптомы со стороны руки, клинические признаки синдрома грудного выхода или отсутствие ответа на вмешательства выше по течению 26
- Провокационные пробы – МРВ/МРА с поднятыми руками способны выявить рёберно-ключичную венозную компрессию, упускаемую при исследовании в покое
Тщательно собранный анамнез не менее важен, чем визуализация. Позиционные головные боли, шум в ушах при поворотах головы, ощущение давления в шее, симптомы со стороны руки, мозговой туман после нагрузки, усиление головной боли в положении лёжа, личный или семейный анамнез гипермобильности – все эти признаки склоняют дифференциальный диагноз в сторону механической проблемы венозного оттока.
Следствия для лечения
Лечение должно соответствовать причине. Из модели венозного оттока вытекает несколько принципов:
- Ацетазоламид и снижение веса уменьшают, соответственно, выработку ликвора и центральное венозное давление. Они помогают, но не устраняют механическую обструкцию.
- Люмбоперитонеальное и вентрикулоперитонеальное шунтирование воздействует на симптом (повышенное давление ликвора), не устраняя причину. Долгосрочные показатели несостоятельности высоки.
- Хирургическая декомпрессия при стилогенной компрессии ВЯВ – удаление шиловидного отростка, поперечного отростка C1 или того и другого с устранением мягкотканных компрессоров – напрямую воздействует на причину выше по течению. В отдельных сериях случаев показана нормализация внутричерепного давления и регресс отёка диска зрительного нерва 16 20
- Резекция первого ребра и декомпрессия грудного выхода воздействуют на компонент ниже по течению, когда лимитирующим узким местом является рёберно-ключичное пространство. Сорок лет клинических данных – от оригинальной серии Raskin 1985 года до серии случаев Cha 2025 года – документируют существенное уменьшение головной боли после этой операции у тщательно отобранных пациентов 27 28 PURED-методика, разработанная мной, позволяет выполнить полную резекцию первого ребра из заднего доступа со значительно лучшим обзором венозных и нервных структур по сравнению с традиционными надключичным и трансаксиллярным подходами.
- Последовательная этапная декомпрессия иногда необходима у пациентов с наслоившимися компрессиями. Принцип такой же, как в сосудистой хирургии в целом: сначала устранить наиболее гемодинамически значимое поражение, затем переоценить ситуацию и заняться следующим.
Хирургическое лечение требуется не каждому пациенту с ИВГ. Но каждый пациент с ИВГ заслуживает обследования, способного выявить механическую причину при её наличии – а у значительной части пациентов она присутствует.
Переосмысление подхода к ИВГ
Метку «идиопатическая внутричерепная гипертензия» следует понимать ровно так, как она устроена: это временный ярлык, отражающий пределы стандартного обследования, а не окончательный диагноз. Когда тракт венозного оттока тщательно изучается – от яремного отверстия, через коридор C1, вниз по динамическому шейному отрезку и через грудной выход – механическая причина выявляется у значительной части пациентов 5 20 26
Компрессия яремной вены на уровне C1 и синдром грудного выхода – два наиболее часто упускаемых из виду фактора. У них общий клинический фенотип, они часто сосуществуют и формируют картину, неотличимую от «классической» ИВГ. Механистический аргумент уже не относится к области предположений: анатомическая работа Ahn документирует стеноз ВЯВ на уровне грудного выхода у троих из каждых четырёх пациентов с нейрогенной формой синдрома 26 случай Chahwala демонстрирует ретроградный кровоток в систему венозного оттока от мозга на венографии в реальном времени 25 а сорок лет хирургических данных – от Raskin до Cha – документируют, что декомпрессия грудного выхода уменьшает обусловленные им головные боли 27 28 Распознавание таких пациентов требует готовности заглянуть за пределы черепа и визуализировать тракт венозного оттока в динамике. Лечение требует мультидисциплинарной экспертизы, объединяющей нейрохирургию, сосудистую хирургию и нейроинтервенционные методы – именно того подхода, на котором построена работа нашей клиники.
Если вам поставили диагноз ИВГ, ваши симптомы не улучшаются и никто не визуализировал ваши яремные вены и грудной выход – этот разговор стоит того, чтобы его начать.
Смотрите также
Литература
- Friedman DI, Liu GT, Digre KB. Revised diagnostic criteria for the pseudotumor cerebri syndrome in adults and children. Neurology. 2013;81(13):1159–1165. doi:10.1212/WNL.0b013e3182a55f17[↩][↩]
- Markey KA, Mollan SP, Jensen RH, Sinclair AJ. Understanding idiopathic intracranial hypertension: mechanisms, management, and future directions. Lancet Neurol. 2016;15(1):78–91. doi:10.1016/S1474-4422(15)00298-7[↩][↩]
- Mollan SP, Davies B, Silver NC, et al. Idiopathic intracranial hypertension: consensus guidelines on management. J Neurol Neurosurg Psychiatry. 2018;89(10):1088–1100. doi:10.1136/jnnp-2017-317440[↩][↩][↩][↩]
- Wall M, Kupersmith MJ, Kieburtz KD, et al. The Idiopathic Intracranial Hypertension Treatment Trial: clinical profile at baseline. JAMA Neurol. 2014;71(6):693–701. doi:10.1001/jamaneurol.2014.133[↩]
- Fargen KM, Midtlien JP, Margraf CR, Hui FK. Idiopathic intracranial hypertension pathogenesis: The jugular hypothesis. Interv Neuroradiol. 2024 Aug 8:15910199241270660. doi:10.1177/15910199241270660[↩][↩][↩][↩][↩][↩][↩][↩][↩]
- Townsend RK, Fargen KM. Intracranial venous hypertension and venous sinus stenting in the modern management of idiopathic intracranial hypertension. Life (Basel). 2021;11(6):508. doi:10.3390/life11060508[↩]
- Bono F, Messina D, Giliberto C, et al. Bilateral transverse sinus stenosis predicts IIH without papilledema in patients with migraine. Neurology. 2006;67(3):419–423. doi:10.1212/01.wnl.0000227892.67354.85[↩]
- Mollan SP, Aguiar M, Evison F, Frew E, Sinclair AJ. The expanding burden of idiopathic intracranial hypertension. Eye (Lond). 2019;33(3):478–485. doi:10.1038/s41433-018-0238-5[↩][↩]
- Corbett JJ, Digre K. Idiopathic intracranial hypertension: an answer to «the chicken or the egg?» Neurology. 2002;58(1):5–6. doi:10.1212/wnl.58.1.5[↩]
- King JO, Mitchell PJ, Thomson KR, Tress BM. Manometry combined with cervical puncture in idiopathic intracranial hypertension. Neurology. 2002;58(1):26–30. doi:10.1212/wnl.58.1.26[↩]
- Scoffings DJ, Pickard JD, Higgins JN. Resolution of transverse sinus stenoses immediately after CSF withdrawal in idiopathic intracranial hypertension. J Neurol Neurosurg Psychiatry. 2007;78(8):911–912. doi:10.1136/jnnp.2006.111765[↩]
- Bono F, Giliberto C, Mastrandrea C, Cristiano D, Lavano A, Fera F, Quattrone A. Transverse sinus stenoses persist after normalization of the CSF pressure in IIH. Neurology. 2005;65(7):1090–1093. doi:10.1212/01.wnl.0000178889.63571.e5[↩]
- De Simone R, Ranieri A, Montella S, Bilo L, Cautiero F. The role of dural sinus stenosis in idiopathic intracranial hypertension pathogenesis: the self-limiting venous collapse feedback-loop model. Panminerva Med. 2014;56(3):201–209.[↩]
- Lim J, Monteiro A, Kuo CC, Jacoby WT, Cappuzzo JM, Becker AB, Davies JM, Snyder KV, Levy EI, Siddiqui AH. Stenting for Venous Sinus Stenosis in Patients With Idiopathic Intracranial Hypertension: An Updated Systematic Review and Meta-Analysis of the Literature. Neurosurgery. 2024;94(4):648–656. doi:10.1227/neu.0000000000002718[↩]
- Ahmed RM, Wilkinson M, Parker GD, Thurtell MJ, Macdonald J, McCluskey PJ, Allan R, Dunne V, Hanlon M, Owler BK, Halmagyi GM. Transverse Sinus Stenting for Idiopathic Intracranial Hypertension: A Review of 52 Patients and of Model Predictions. AJNR Am J Neuroradiol. 2011;32(8):1408–1414. doi:10.3174/ajnr.A2575[↩]
- Mejia-Vergara AJ, Sultan W, Kostas A, Mulholland CB, Sadun A. Styloidogenic Jugular Venous Compression Syndrome with Papilloedema: Case Report and Review of the Literature. Neuroophthalmology. 2021;46(1):54–58. doi:10.1080/01658107.2021.1887288[↩][↩][↩]
- Dashti SR, Nakaji P, Hu YC, et al. Styloidogenic jugular venous compression syndrome: diagnosis and treatment: case report. Neurosurgery. 2012;70(3):E795 – E799. doi:10.1227/NEU.0b013e3182333859[↩][↩]
- Pokeerbux MR, Delmaire C, Morell-Dubois S, Demondion X, Lambert M. Styloidogenic compression of the internal jugular vein, a new venous entrapment syndrome? Vasc Med. 2020;25(4):378–380. doi:10.1177/1358863X20902842[↩][↩]
- Scerrati A, Norri N, Mongardi L, et al. Styloidogenic-cervical spondylotic internal jugular venous compression, a vascular disease related to several clinical neurological manifestations: diagnosis and treatment – a comprehensive literature review. Ann Transl Med. 2021;9(8):718. doi:10.21037/atm-20-7698[↩][↩]
- Zhou D, Meng R, Zhang X, et al. Intracranial hypertension induced by internal jugular vein stenosis can be resolved by stenting. Eur J Neurol. 2018;25(2):365-e13. doi:10.1111/ene.13512[↩][↩][↩][↩]
- Holmlund P, Johansson E, Qvarlander S, Wåhlin A, Ambarki K, Koskinen LO, Malm J, Eklund A. Human jugular vein collapse in the upright posture: implications for postural intracranial pressure regulation. Fluids Barriers CNS. 2017;14:17. doi:10.1186/s12987-017-0065-2[↩][↩]
- San Millán Ruíz D, Gailloud P, Rüfenacht DA, Delavelle J, Henry F, Fasel JH. The craniocervical venous system in relation to cerebral venous drainage. AJNR Am J Neuroradiol. 2002;23(9):1500–1508.[↩]
- Gisolf J, van Lieshout JJ, van Heusden K, Pott F, Stok WJ, Karemaker JM. Human cerebral venous outflow pathway depends on posture and central venous pressure. J Physiol. 2004;560(Pt 1):317–327. doi:10.1113/jphysiol.2004.070409[↩]
- Marini TJ, Chughtai K, Nuffer Z, Hobbs SK, Kaproth-Joslin K. Blood finds a way: pictorial review of thoracic collateral vessels. Insights Imaging. 2019;10(1):63. doi:10.1186/s13244-019-0753-3[↩][↩]
- Chahwala V, Tashiro J, Li X, Baqai A, Rey J, Robinson HR. Venous Thoracic Outlet Syndrome as a Cause of Intractable Migraines. Ann Vasc Surg. 2017;39:285.e5–285.e8. doi:10.1016/j.avsg.2016.05.109[↩][↩][↩]
- Ahn SS, Miller TJ, Chen SW, Chen JF. Internal jugular vein stenosis is common in patients presenting with neurogenic thoracic outlet syndrome. Ann Vasc Surg. 2014;28(4):946–950. doi:10.1016/j.avsg.2013.12.009[↩][↩][↩][↩][↩]
- Raskin NH, Howard MW, Ehrenfeld WK. Headache as the leading symptom of the thoracic outlet syndrome. Headache. 1985;25(4):208–210. doi:10.1111/j.1526-4610.1985.hed2504208.x[↩][↩][↩][↩]
- Cha YH, Randall L, Weber J, Ahn S. Treatment of thoracic outlet syndrome to relieve chronic migraine. Clin Anat. 2025;38(3):314–323. doi:10.1002/ca.24242[↩][↩][↩][↩][↩]
- Midtlien JP, Curry BP, Chang E, et al. Characterizing a new clinical phenotype: the co-existence of cerebral venous outflow and connective tissue disorders. Front Neurol. 2023;14:1305972. doi:10.3389/fneur.2023.1305972[↩]
- Manupipatpong S, Primiani CT, Fargen KM, et al. Jugular venous narrowing and spontaneous spinal cerebrospinal fluid leaks: A case – control study exploring association and proposed mechanism. Interv Neuroradiol. 2024;30(6):812–818. doi:10.1177/15910199241287417[↩]
