ظلّ ارتفاع ضغط الدماغ مجهول السبب – ويُعرف أيضاً بـالورم الدماغي الكاذب – يحمل لعقود اسماً يقول عملياً للمريض إن سبب ما يحدث غير معروف. تُعرَّف الحالة بارتفاع ضغط السائل الدماغي الشوكي (السائل النخاعي) في غياب ورم دماغي أو استسقاء أو سبب بنيوي واضح آخر 1 والمرضى عادةً مصابون بالسمنة، إناث، في سن الإنجاب 2 3 ويُراجعون بصداع منهك، وطنين نابض، ووذمة حليمة العصب البصري، وتشوش رؤية عابر، وفقدان بصر تدريجي 4
تُحمّل الرواية الكلاسيكية المسؤولية للسمنة والهرمونات وخللٍ مبهم في إعادة امتصاص السائل النخاعي. لكن في الممارسة السريرية الحقيقية، تترك هذه الرواية كثيراً من المرضى دون أجوبة ودون علاج فعّال طويل الأمد. وتُظهر مجموعة متنامية من الأدلة أن الضغط المرتفع لدى نسبة كبيرة من المرضى ليس مجهول السبب على الإطلاق – بل هو نتيجة انسداد ميكانيكي للتصريف الوريدي للدماغ 5 6 7
اثنان من أكثر مواضع الانسداد إغفالاً يقعان في نقاط تشريحية ضيّقة جداً: الوريد الوداجي الباطن عند الفقرة العنقية الأولى (C1)، والممر الوريدي تحت الترقوة – العضدي الرأسي عند مخرج الصدر. ينبغي أن يكون هذان الموضعان في التشخيص التفريقي لكل مريض شُخِّص بارتفاع ضغط الدماغ، لا سيما من تستمر أعراضهم رغم إنقاص الوزن، والأسيتازولاميد، والبزل القطني، وتحويلات السائل النخاعي، بل وحتى دعامات الجيب الوريدي.
يشرح هذا المقال المنطق والتشريح والأدلة الداعمة والمآلات العملية لهذا الطرح.
ما هو ارتفاع ضغط الدماغ – تذكير موجز
المعيار التشخيصي المعتمد حالياً هو معايير فريدمان 2013، التي تشترط 1
- أعراض وعلامات ارتفاع ضغط داخل الجمجمة المنتشر أو وذمة حليمة العصب البصري
- فحص عصبي طبيعي عدا اضطرابات الأعصاب القحفية
- تصوير عصبي طبيعي (لا كتلة، ولا استسقاء، ولا آفة بنيوية)
- تركيب طبيعي للسائل النخاعي
- ارتفاع ضغط فتح البزل القطني (>25 سم ماء عند البالغين، >28 سم ماء عند الأطفال)
إذا تم التعرف على أي سبب – تخثر الجيوب الجافوية، بعض الأدوية، مرض الغدد الصمّ – يُعاد تصنيف الحالة بوصفها ارتفاعاً ثانوياً لضغط الدماغ، وتسقط عنها صفة «مجهول السبب». المشكلة أنه في النموذج السائد حالياً، نادراً ما يبحث الأطباء عن انسداد وريدي خارج الجمجمة. يتوقف التصوير القياسي عند قاعدة الجمجمة، ويكون المريض في وضع الاستلقاء على الظهر والرأس مستقيم أثناء الفحص؛ أما التضيقات الديناميكية التي لا تظهر إلا في الوضع المنتصب أو مع تدوير الرأس، فتبقى غير مرئية.
النتيجة متوقَّعة: مريضٌ لديه سبب ميكانيكي قابل للتحديد بوضوح يُوسَم بـ«مجهول السبب» ويُعالَج بشكل عَرَضي.
الديموغرافيا الكلاسيكية لا تزال صحيحة – لكنها لا تروي القصة كاملة
- يصيب ارتفاع ضغط الدماغ النساء بمعدل يزيد تسع مرات تقريباً عن الرجال 3
- تتمركز ذروة الإصابة بين سنّي 20 و40 عاماً 3
- أقوى عامل خطر معروف كلاسيكياً هو السمنة، الموجودة لدى 70–94% من المرضى 2
- يصاب ما يصل إلى 40% من المرضى بضعف بصر دائم، ويُصبح 1–10% منهم مكفوفين قانونياً 3
هذه الأرقام حقيقية، والسمنة تلعب دوراً فعلياً – فارتفاع الضغط داخل البطن والضغط الوريدي المركزي يرفعان فعلاً الضغط الوريدي داخل الجمجمة 5 لكن السمنة وحدها لا تفسّر المريض النحيل المصاب بارتفاع ضغط الدماغ، ولا المريض ذا المرض المقاوم رغم إنقاص الوزن، ولا المريض الذي يعاني ارتفاع ضغط الدماغ مجهول السبب دون وذمة حليمة العصب البصري (IIHWOP) 8
فرضية الوريد الوداجي – نموذج موحِّد
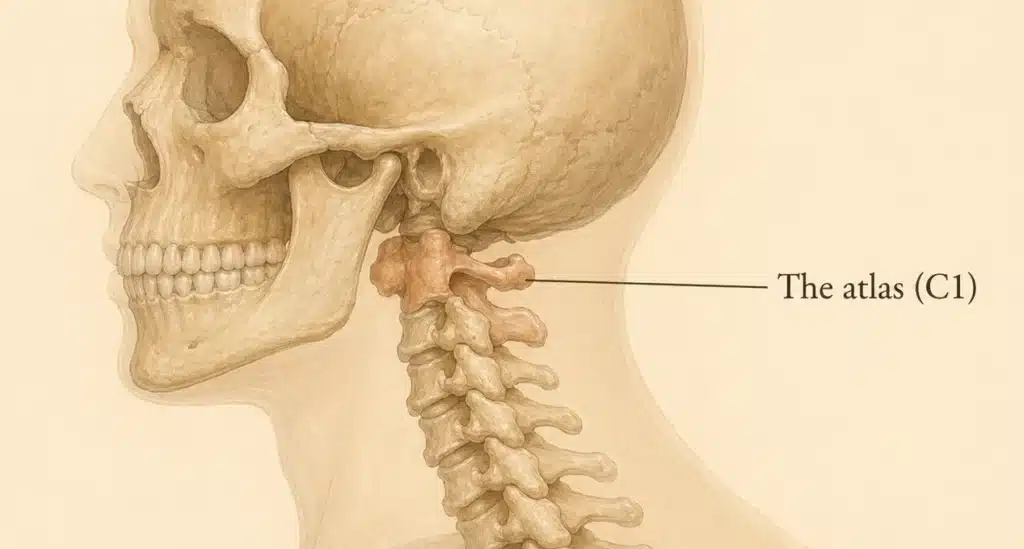
في عام 2024، نشر فارغن وميدتلين ومارغراف وهوي إعادة الصياغة الأهم لمرضية ارتفاع ضغط الدماغ في الفترة الأخيرة: فرضية الوريد الوداجي 5 تذهب الحجة المركزية لدى المؤلفين إلى أن ارتفاع ضغط الدماغ واضطرابات طيفه يُفهَمان أفضل ما يُفهَمان بوصفهما مشكلة في التصريف الوريدي للدماغ، يلعب فيها الوريدان الوداجيان الباطنان (IJV) الدور الأولي والمهمل في كثير من الأحيان.
يمكن تلخيص النموذج في ست نقاط 5
- الوريدان الوداجيان الباطنان عرضةٌ للانضغاط الفسيولوجي والمرضي على طول مسارهما بالكامل – عند الفقرة C1 من قِبَل الناتئ الإبري، وبين الفقرتين C3 وC6 من قِبَل قوى عضلية وسُباتية ديناميكية.
- التضيق الديناميكي الشديد في الوريد الوداجي الباطن، مع تدرّجات ضغط عنقية كبيرة، شائع في مرضى طيف ارتفاع ضغط الدماغ، ويؤثر تأثيراً ملحوظاً في الضغط الوريدي داخل الجمجمة وضغط السائل النخاعي.
- مسارات الدوران الجانبي خارج الوريد الوداجي تتوسع مع الزمن، لكنها تبقى غير كافية لتعويض التصريف الوداجي الطبيعي.
- ضعف التصريف عبر الوريد الوداجي الباطن يُفضي إلى ارتفاع الضغط الوريدي داخل الجمجمة واحتقانه، فيرفع ضغط السائل النخاعي والضغط داخل الجمجمة (ICP).
- تتعرض المنظومة الغليمفاوية للاحتقان أيضاً، لكنها لا تستطيع التعويض.
- يُفضي ارتفاع الضغط داخل الجمجمة المستمر في النهاية إلى انضغاط الجيب المستعرض من خارج جداره – الموجودة الكلاسيكية على التصوير – والتي تعمل مُضخِّماً للعملية، لا سبباً أولياً لها.
النقطة الأخيرة أساسية ويُساء تفسيرها بانتظام في الممارسة السريرية. تضيق الجيب المستعرض في تصوير الأوردة بالرنين المغناطيسي هو الموجودة التي هيمنت على تقييم ارتفاع ضغط الدماغ طوال عقدين، في حين أن الانسداد الأقرب إلى المنبع – والأهم فسيولوجياً – على مستوى الوريد الوداجي الباطن، يكاد لا يُذكر في تقرير التصوير. ينصبّ الانتباه السريري على النتيجة في مجرى التدفق دون السبب أعلاه. وقد طُرح سؤال «الدجاجة أم البيضة» رسمياً لأول مرة بواسطة كوربيت وديغري عام 2002 9 ومنذ ذلك الحين أصبح الجواب واضحاً نسبياً. أظهر كنغ وزملاؤه في العام نفسه أن خفض ضغط السائل النخاعي عبر بزل عنقي جانبي C1 – C2 يُزيل فوراً ارتفاع ضغط الجيب الوريدي المُقاس بقياس الضغط المباشر 10– وهي ملاحظة لا تتوافق جوهرياً مع كون التضيق هو السبب الأولي في المنبع. وأكدت دراسات التصوير اللاحقة الموجودة نفسها مراراً: تتراجع تضيقات الجيوب المستعرضة في تصوير الأوردة بالقسطرة وبالأشعة المقطعية، أحياناً خلال ساعة، بعد سحب السائل النخاعي أو إجراء التحويلة 11
ومن باب الإنصاف، لا تُعدّ القابلية للتراجع شاملةً. تابع بونو وزملاؤه أربعة عشر مريضاً بارتفاع ضغط الدماغ مع تضيق ثنائي للجيوب المستعرضة عبر تصوير أوردة بالرنين المغناطيسي تسلسلي على مدى ست سنوات، ووجدوا أن التضيقات استمرت حتى لدى تسعة مرضى (64%) طبّع ضغط السائل النخاعي لديهم بالعلاج الدوائي 12– ما يشير إلى أن الجيب يخضع في مجموعة فرعية من الحالات لإعادة تشكيل بنيوي يُفقده الاستجابة لمجرد خفض الضغط داخل الجمجمة. ولّخص دي سيموني وزملاؤه هذه الملاحظات المتباينة في نموذج حلقة تغذية راجعة ذاتية التحديد للانهيار الوريدي: ارتفاع أوّلي في ضغط السائل النخاعي يضغط جزءاً من الجيب قابلاً للانهيار، فيُسهم الارتفاع الناجم في الضغط الوريدي في تقليل إعادة امتصاص السائل النخاعي، فيستقرّ الضغطان عند توازن جديد أعلى 13 يستوعب هذا النموذج كلا النمطين: في بعض المرضى تُكسَر الحلقة بسحب حادّ للسائل النخاعي فيتراجع التضيق، وفي آخرين، ولا سيما في المرض الطويل الأمد، يترسّخ التوازن ويستمر التضيق رغم تطبيع الضغط. وفي كل الأحوال، يبقى تضيق الجيب المستعرض مشاركاً مُضخِّماً لذاته، لا السبب الأصلي.
ولهذا تحديداً ينتكس عدد كبير من المرضى بعد دعامات الجيب الوريدي. أفادت مراجعة منهجية وتحليل تلوي عام 2024 لـ 694 مريضاً بارتفاع ضغط الدماغ من 24 دراسة بـمعدل تضيق متكرر مجمَّع قدره 17.7%، وأن 22.3% من المرضى استمرت أعراضهم أو ساءت بعد الدعامة، وخلص المؤلفون إلى أن هذه المعدلات تُبرز الحاجة إلى مزيد من البحث في الإجراء 14 وفي دراسة أتراب أقدم، تابع أحمد وزملاؤه 52 مريضاً بارتفاع ضغط الدماغ بعد دعامة الجيب المستعرض، وأبلغوا عن انتكاس أعراض لدى 6 مرضى (11.5%) نتيجة ارتفاع ضغط وريدي وتضيق جديد ملاصق للدعامة الأصلية، استلزم إجراء دعامة ثانية؛ احتاج أحد المرضى في النهاية إلى أربع 15 تُبقي الدعامة النتيجة مفتوحة، فيما يبقى الانسداد في المنبع – على مستوى الوريد الوداجي أو ما هو أبعد منه – دون مساس 5
نقطة الانضغاط الأولى: تضيق الوريد الوداجي الباطن عند الفقرة C1 (الانضغاط الإبري الوداجي)
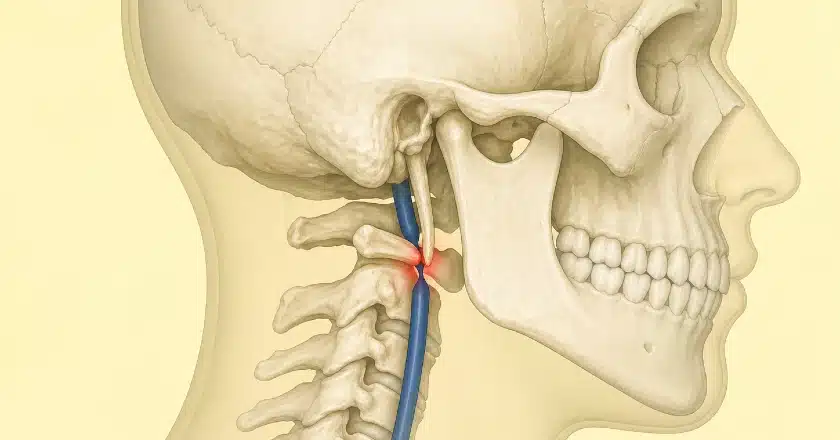
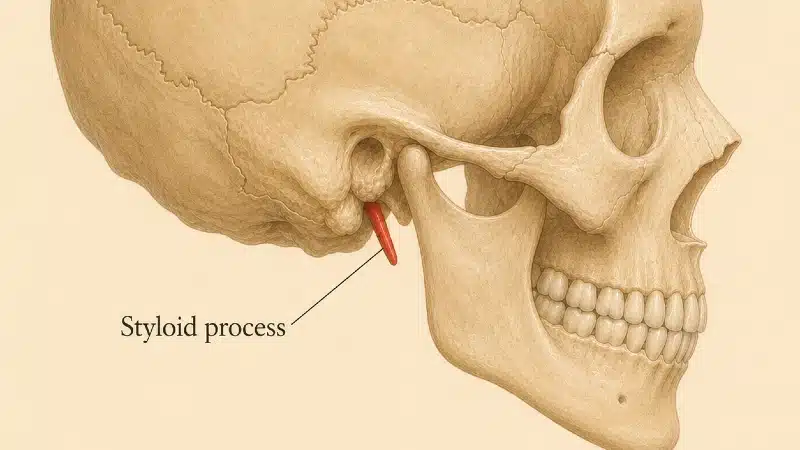
يخرج الوريد الوداجي الباطن من الجمجمة عبر الثقبة الوداجية ويدخل مباشرة في ممر ضيق بين بنيتين صلبتين: الناتئ الإبري للعظم الصدغي من الأمام، والناتئ المستعرض للفقرة العنقية الأولى (C1، الأطلس) من الخلف. عند بعض الأفراد، يكون هذا الممر ضيقاً إلى درجة تُسبّب انضغاطاً ميكانيكياً للوريد – وهي ظاهرة تُعرف بـمتلازمة الانضغاط الإبري للوريد الوداجي 16 17 18 19
والتشبيه: خرطوم حديقة معصور بين صخرتين. حتى الناتئ الإبري ذو الطول الطبيعي نسبياً قد يُحدث تضيقاً واضحاً إذا كان متجهاً نحو الإنسي، أو إذا كان الناتئ المستعرض للفقرة C1 أكبر من المعتاد أو موضوعاً جانبياً 18 ومن المساهمين في الانضغاط من الأنسجة الرخوة – العضلة ذات البطنين، والشريان القفوي الذي يلتفّ حول الوريد، والعضلات المستقيمة للرأس، والأشرطة الليفية داخل غمد السباتي – كل هذه تزيد الانسداد 19
لماذا يهمّ انضغاط C1 في ارتفاع ضغط الدماغ
عندما ينضغط الوريد الوداجي الباطن عند الفقرة C1، يتراكم الدم في الجيوب الوريدية الجافوية، ويرتفع الضغط الوريدي في الدماغ. وبما أن إعادة امتصاص السائل النخاعي تعتمد على تدرّج ضغط بمقدار 3 إلى 5 ملم زئبق تقريباً بين السائل النخاعي ودم الجيب الوريدي 5 فإن أي ارتفاع في الضغط الوريدي يفرض ارتفاعاً تعويضياً في ضغط السائل النخاعي. تتطور لدى المريض صداع، وطنين نابض، ووذمة حليمة العصب البصري، وتشوش رؤية عابر، وضباب ذهني – ويُوسَم بارتفاع ضغط الدماغ.
وقد أظهرت مجموعات متعددة الآن أن رفع الانسداد الوداجي يحلّ ارتفاع ضغط الدماغ لدى مرضى منتقين بعناية، مع تطبيع ضغوط الفتح وانحسار الأعراض 20 تظل إزالة الضغط جراحياً – استئصال الناتئ الإبري، أو الناتئ المستعرض للفقرة C1، أو كليهما، مع تحرير أي ضواغط من الأنسجة الرخوة – هي المقاربة الأكثر منطقية ودواماً، لأنها تعالج السبب الميكانيكي الفعلي بدلاً من أن تَضْطرّ الوريد للبقاء مفتوحاً ضد قوة خارجية لا ترخي.
العلامة التي يغفلها معظم الأطباء: الأعراض الوضعية
انضغاط الوريد الوداجي الباطن عند الفقرة C1 ديناميكي. يشتد بحركة الرقبة، ويزداد عند استلقاء المريض على ظهره – لأن هذا الوريد هو المسار المهيمن لتصريف الدماغ في وضع الاستلقاء. المريض الذي يكون صداعه أشدّ ما يكون عند الاستيقاظ، الذي ينام شبه جالس بدافع غريزي، الذي يختفي طنينه عند الضغط اليدوي على الرقبة، الذي يلاحظ ضباباً ذهنياً بعد تدوير الرأس – هذا المريض يصف سمات ميكانيكية، لا سمات صداع نصفي.
نقطة الانضغاط الثانية: مخرج الصدر – طبقة منسيّة
هنا تصبح المحادثة أكثر إثارة، وهنا يبدأ الأدب الطبي حديثاً في اللحاق بالموضوع.
لا يصبّ الوريد الوداجي الباطن مباشرة في القلب. بل يتحد مع الوريد تحت الترقوة خلف الطرف الإنسي للترقوة ليُكوّنا الوريد العضدي الرأسي (الوريد المسمى)، الذي يعبر بدوره الجزء العلوي من المنصف ليصل إلى الوريد الأجوف العلوي. يمرّ هذا المقطع كاملاً – من الترقوة الإنسية إلى الوريد الأجوف العلوي – عبر مخرج الصدر، النقطة التشريحية الضيقة ذاتها التي تنتج عنها متلازمة مخرج الصدر.
يفكر معظم الأطباء في متلازمة مخرج الصدر بوصفها مشكلة في الضفيرة العضدية أو الشريان تحت الترقوة. هذا التعليم القياسي صحيح بقدر ما هو – تُمثّل المتلازمة العصبية 80–85% من الحالات. لكن المكوّن الوريدي أوسع انتشاراً مما توحي به الكتب المرجعية، وعواقبه تتجاوز الذراع بكثير.
الشبكة الوريدية خارج الوداجية
الأوردة الوداجية الباطنة هي المسار المهيمن للتصريف الوريدي للدماغ في وضع الاستلقاء على الظهر. أما في الوضع المنتصب، فترتفع هذه الأوردة فوق مستوى القلب وتنهار تحت الضغط الجوي، فتتوقف عن أداء وظيفة قناة التدفق الأساسية 21 عندئذٍ يتحول الدم الوريدي للدماغ إلى نظام بديل: الشبكة الوريدية خارج الوداجية (EJN).
تشمل الشبكة الوريدية خارج الوداجية: الضفيرة الوريدية الفقرية (الداخلية والخارجية)، والأوردة العنقية العميقة، والوريد الوداجي الظاهر، والأوردة المُرسِلة في الحفرة القحفية الخلفية. وعند قاعدة الجمجمة، يرتبط المساران تشريحياً عبر ملتقى تروالار اللقمي الأمامي (ACC) – محور وريدي عند الفتحة الخارجية للقناة تحت اللسانية، يربط لمبة الوريد الوداجي مباشرةً بالضفيرة الفقرية عبر الأوردة اللقمية 22 وأظهرت النمذجة الرياضية ودراسات التصوير في الوضع المنتصب أن الضفيرة الفقرية تصبح في الوضع المنتصب مسار التدفق المهيمن للدم الوريدي للدماغ، فيما يحمل الوريدان الوداجيان الباطنان حصة صغرى 21 23 يعمل النظامان بوصفهما دارتين متوازيتين تلتقيان عند نقطة الانتهاء التشريحية ذاتها: الأوردة تحت الترقوة والعضدية الرأسية عند قاعدة الرقبة.
كيف تُرهق متلازمة مخرج الصدر التصريف الوريدي للدماغ
التقاء هذين النظامين عند قاعدة الرقبة هو ما يربط متلازمة مخرج الصدر بضغط الدماغ. عندما ينضغط الوريد تحت الترقوة بشكل مزمن في موضع التقاء الترقوة بالضلع الأول، لا يستطيع الدم القادم من الطرف العلوي العودة عبر المقطع المنسد، فيُجبَر على المسارات الجانبية.
يوثّق الأدب الطبي المنهجي للتصوير بدقةٍ إلى أين تذهب هذه الجوانب. في المراجعة المصوّرة لأنماط الجوانب الصدرية لماريني وزملائه، تُحدَّد القنوات الوريدية العنقية بوصفها المنطقة الجانبية الأساسية لانسداد الإبط وما تحت الترقوة 24 وتشمل المسارات الأمامية المُسمّاة في الرقبة: الوريد الوداجي الباطن، الوريد الوداجي الظاهر، القوس الوريدية الوداجية، الوريد الدرقي السفلي، والضفيرة الوريدية الفقرية. أما الجوانب الخلفية في الرقبة – التي توصف بأنها أكثر شيوعاً وأكثر بروزاً – فتمرّ عبر الضفيرة الفقرية ذاتها وقد تعبر إلى الجانب المقابل، أو تصبّ في جدار الصدر ونظام الوريد الفردي 24
هذه القنوات الجانبية هي بالضبط الأوعية التي تتألف منها الشبكة الوريدية خارج الوداجية المسؤولة عن تصريف الدماغ. لذلك تقوم الشبكة لدى مريض المتلازمة الوريدية لمخرج الصدر بوظيفتين في آن واحد: تصريف الطرف العلوي عبر تدفق جانبي عكسي، وتصريف الدماغ. في وضع الاستلقاء، تكون الأوردة الوداجية الباطنة مفتوحةً وتحمل غالبية العود الوريدي الدماغي، وقد تُحتمل هذه المطالبة المزدوجة. أما في الوضع المنتصب، حين تنهار الأوردة الوداجية الباطنة ويصبح الدماغ معتمداً فسيولوجياً على الشبكة خارج الوداجية، يَنْفَجِر النظام تحت الحمل. لا يستطيع الدم الوريدي للدماغ التصريف بكفاءة عبر قنوات سبق أن احتقنت بتدفق جانبي عكسي قادم من تحت الترقوة. والنتيجة: اختلال التصريف الوريدي للدماغ، وارتفاع الضغط الوريدي الدماغي، ومن خلال آلية إعادة امتصاص السائل النخاعي المعتمدة على الضغط – ارتفاع الضغط داخل الجمجمة.
ولقد التُقط هذا التحويل في التدفق مباشرةً على التصوير. في عام 2017، وصف شَهْوالة وزملاؤه مريضةً تعاني صداعاً نصفياً منهكاً سبقه تورم في ذراع واحدة. في تصوير الأوردة الديناميكي، ومع تقريب الذراع، تدفق الصبغ المحقون في الوريد تحت الترقوة بشكل عكسي إلى الوريد الوداجي الباطن في الجانب نفسه، مع قنوات جانبية واسعة تحوّل الدم نحو الرأس 25 تعافت المريضة من الصداع النصفي تماماً بعد استئصال العضلة الأخمعية واستئصال الضلع الأول. هذه الحالة هي البرهان الأنغرافي الأكثر مباشرةً في الأدب المنشور على أن الانسداد الوريدي عند ملتقى الترقوة بالضلع الأول قادر على إجبار العود الوريدي القادم من الذراع إلى مسار التصريف الدماغي.
ويتسق الانتشار العالي لشذوذات الوريد الوداجي الباطن لدى مرضى متلازمة مخرج الصدر في تصوير الأوردة الروتيني مع هذه الفسيولوجيا. في دراسة تصوير أوردة استباقية لمرضى متتاليين بمتلازمة مخرج الصدر العصبية، وجد أهن وزملاؤه تضيقاً في الوريد الوداجي الباطن لدى 76.2% (ثنائي لدى 47.6%)، إلى جانب تضيق في الوريد تحت الترقوة لدى 82.5% 26 الوريد الوداجي الباطن المُجنَّد بوصفه قناة جانبية عكسية لنظام تحت الترقوة المنسدّ يُتوقَّع أن يبدو متضيّقاً ومحاطاً بقنوات جانبية شاذة في حقن الصبغ، سواء كانت المشكلة الأساسية انضغاطاً ثابتاً أو احتقاناً وظيفياً.
أربعون عاماً من الأدلة السريرية – جراحة متلازمة مخرج الصدر تُحسّن الصداع المعنّد
الحجة بأن متلازمة مخرج الصدر تُسهم في ارتفاع الضغط داخل الجمجمة ليست جديدة. هي في الواقع حجة عمرها أربعة عقود – لكن الأدب الطبي ظلّ موزعاً بين جراحة الأوعية الدموية، وعلم الأعصاب، وطب أعصاب العين، ولم يُجمع بعدُ في الإطار الذي يستحقه.
في عام 1985، تابع راسكين، هاوارد، وإهرنفيلد ثلاثين مريضاً متتالياً بمتلازمة مخرج الصدر لمدة ستة أشهر على الأقل بعد استئصال الضلع الأول عبر الإبط. كان لدى ستة وعشرين منهم صداع متكرر سبق ظهور آلام الرقبة والكتف. وبعد الجراحة، تخلّص ثلاثة عشر مريضاً تماماً من الصداع، عاد أحد عشر مريضاً كانوا عاجزين عن العمل إلى وظائفهم، وأبلغ أحد عشر آخرون عن استجابة جديدة لأدوية فعّالة على الأوعية كانت غير فعّالة قبل الجراحة 27 في ذلك الوقت، عُزيت الآلية إلى «عوامل وعائية» مبهمة. أما اليوم فلدينا صورة تصوير أنغرافي أوضح بكثير لماهية تلك العوامل، كما أظهرت حالة شَهْوالة 2017 المذكورة أعلاه.
أحدث وأكبر سلسلة، نشرها تشا وزملاؤه في 2025 في مجلة Clinical Anatomy، فحصت خمسين مريضاً متتالياً يحملون التشخيص المزدوج للصداع النصفي المزمن ومتلازمة مخرج الصدر 28 كانت السمات السريرية كاشفة:
- الصداع كان مقتصراً على جانب واحد أو أشد على الجانب نفسه لطرف المتلازمة لدى 76% من المرضى
- تورم الطرف كان مرافقاً لدى 67%
- ومن أكثر العلامات تشخيصياً – 84% أبلغوا عن صداع يشتدّ بالاستلقاء، وهو بالضبط النمط المتوقع حين يصبح التصريف داخل الجمجمة أثناء النوم معتمداً بشكل متزايد على المسار الوداجي
خضع اثنان وثلاثون من الخمسين لإزالة ضغط جراحية، مع تحسّن جوهري في عبء الصداع 28 تَفاقُم الصداع في وضع الاستلقاء هو البصمة السريرية لمرض اختلال التصريف الوريدي للدماغ. يصف المرضى استيقاظهم بصداع، ونومهم شبه جالسين بدافع غريزي، وأن رفع الرأس يجلب راحة أكبر مما تجلبه الأدوية.
تتجمّع القطع في حكاية واحدة متماسكة تمتد على أربعين عاماً. ملاحظة راسكين السريرية عام 1985 – انحسار الصداع بعد استئصال الضلع الأول 27 برهان أهن التشريحي 2014 – أن 76% من مرضى المتلازمة العصبية يحملون تضيقاً في الوريد الوداجي الباطن 26 برهان شَهْوالة الأنغرافي 2017 – التدفق العكسي إلى المنظومة الوريدية للدماغ من انسداد على مستوى متلازمة مخرج الصدر 25 سلسلة تشا الحديثة 2025 – توثيق السمات السريرية والاستجابة الجراحية في خمسين مريضاً 28 نُشرت كل هذه الأبحاث في مجلات تخصصية مختلفة، ولم يُنجز الحقل بعدُ تركيبها معاً. وهذا التركيب هو ما يحاول هذا المقال إنجازه.
التركيب: نموذج التصريف الوريدي للدماغ ذو المستويين
عندما يُعاد تأطير ارتفاع ضغط الدماغ بوصفه مرض اختلال التصريف الوريدي، تتضح الصورة السريرية بصورة ملموسة. على الدم الوريدي للدماغ أن يجتاز سلسلة من النقاط الضيّقة:
- من الجيوب الجافوية، عبر الثقبة الوداجية
- مروراً بـممر الناتئ الإبري – C1 (نقطة الانضغاط الأولى)
- نزولاً عبر العلاقات العضلية والسباتية الديناميكية على مستوى C3 – C6
- عبر الفراغ الواقع بين الترقوة والضلع الأول عند مخرج الصدر (نقطة الانضغاط الثانية)
- عبر الوريد العضدي الرأسي والوريد الأجوف العلوي إلى الأذين الأيمن
أيّ تضيق على أي من هذه المستويات يرفع الضغط في المنبع، ووجود تضيقات على عدة مستويات يُراكم المشكلة. وبما أن النظام ديناميكي – يتأثر بوضع الرأس والذراع والتنفس والوضعية – فإن التصوير الساكن في وضع الاستلقاء على الظهر يفوّت بانتظام هذه التضيقات المتراكمة.
يفسّر هذا النموذج بعض أكثر الملاحظات إحباطاً في الممارسة:
- لماذا تُتيح إجراءات تصريف السائل النخاعي والأدوية المخفِّضة للضغط راحةً مؤقتةً فقط في كثير من الأحيان – لأنها لا تعالج الانسداد الميكانيكي في المنبع
- لماذا ينتكس بعض المرضى بعد إنقاص الوزن (الانسداد الميكانيكي لا يتأثر بمؤشر كتلة الجسم)
- لماذا يتداخل ارتفاع ضغط الدماغ «مجهول السبب» تداخلاً كبيراً مع متلازمة مخرج الصدر، ومتلازمة إيغل، ومتلازمة تسرع القلب الانتصابي الوضعي (POTS)، ومتلازمة إيلرز – دانلوس (EDS)، وأنماط تسرّب السائل النخاعي 29 30
- لماذا قد تغيب وذمة حليمة العصب البصري (IIHWOP) حين تُعوّض الجوانب جزئياً 8
المآلات التشخيصية – ما الذي ينبغي تصويره
إذا قَدِم المريض بظاهرة ارتفاع ضغط الدماغ، لا ينبغي أن يقتصر التقييم على تصوير الدماغ بالرنين المغناطيسي والبزل القطني. ينبغي أن يشمل التقييم الكامل للتصريف الوريدي ما يلي:
- تصوير الأوردة بالأشعة المقطعية (CT venography) للرأس والرقبة – وهو المعيار الذهبي الحالي لتصوير ممر الناتئ الإبري – C1 وتقدير تضيق الوريد الوداجي 16 17
- تصوير الأوردة بالرنين المغناطيسي (MRV) – مفيد لتقييم أنماط التدفق وحالة الجوانب 5
- التصوير الديناميكي – تصوير في أوضاع متعددة للرأس، وحين أمكن في الوضع المنتصب، لأن الصور الساكنة في وضع الاستلقاء على الظهر تُقلّل من تقدير التضيق الديناميكي 5
- تصوير الأوردة بالقسطرة مع قياس الضغوط – الطريقة الموثوقة الوحيدة لتقدير تدرّجات الضغط عبر التضيق؛ تُعدّ التدرّجات التي تتجاوز 3–5 ملم زئبق عبر التضيق ذات دلالة سريرية 20
- تصوير الأوردة العضدية الرأسية وتحت الترقوة – لا سيما إذا كان لدى المريض أي أعراض في الذراع، أو سمات سريرية لمتلازمة مخرج الصدر، أو لم يستجب للتدخلات في المنبع 26
- المناورات الاستثارية – تصوير الأوردة/الشرايين بالرنين المغناطيسي مع رفع الذراعين قد يكشف عن انضغاط وريدي عند ملتقى الترقوة بالضلع الأول لا تُظهره صور الراحة
التاريخ المرضي الدقيق لا يقلّ أهمية عن التصوير. الصداع الوضعي، والطنين الذي يستثيره تدوير الرأس، والشعور بالضغط في الرقبة، وأعراض الذراع، والضباب الذهني بعد المجهود، وتَفاقُم الصداع بالاستلقاء، والتاريخ الشخصي أو العائلي لفرط حركة المفاصل – تدفع جميعها التشخيص التفريقي نحو مشكلة ميكانيكية في التصريف الوريدي.
المآلات العلاجية
ينبغي أن يلائم العلاج السبب. تنبثق عدة مبادئ من نموذج التصريف الوريدي:
- الأسيتازولاميد وإنقاص الوزن يخفضان على التوالي إنتاج السائل النخاعي والضغط الوريدي المركزي. يساعدان، لكنهما لا يُصلحان الانسداد الميكانيكي.
- التحويلات القَطَنية البريتونية والبطينية البريتونية تعالج العَرَض (ارتفاع ضغط السائل النخاعي) دون معالجة السبب. ومعدلات الإخفاق على المدى الطويل عالية.
- إزالة الضغط جراحياً عن انضغاط الوريد الوداجي الباطن من النوع الإبري – استئصال الناتئ الإبري، أو الناتئ المستعرض للفقرة C1، أو كليهما، مع تحرير ضواغط الأنسجة الرخوة – يعالج السبب الفعلي في المنبع. أظهرت سلاسل حالات مختارة تطبيع الضغط داخل الجمجمة وانحسار وذمة حليمة العصب البصري 16 20
- استئصال الضلع الأول وإزالة الضغط عن مخرج الصدر يعالج المكوّن في المصبّ حين يكون ملتقى الترقوة بالضلع الأول هو نقطة الاختناق. تُوثّق أربعون عاماً من البيانات السريرية – من سلسلة راسكين الأصلية 1985 إلى سلسلة تشا 2025 – تحسناً جوهرياً في الصداع بعد هذا الإجراء عند المرضى المنتقين بشكل ملائم 27 28 يتيح إجراء PURED الذي طوّرته استئصال الضلع الأول كاملاً عبر مدخل خلفي مع وصول أفضل بكثير إلى البنى الوريدية والعصبية مقارنةً بالمداخل التقليدية فوق الترقوة وعبر الإبط.
- إزالة الضغط المرحلية المتتابعة قد تكون ضرورية في المرضى ذوي الانضغاطات المتراكمة. المبدأ هو نفسه في جراحة الأوعية الدموية عموماً: ابدأ بإزالة الآفة الأكثر دلالة على الديناميكا الدموية، ثم أعد التقييم، ثم انتقل إلى التالية.
ليس كل مريض بارتفاع ضغط الدماغ يحتاج إلى جراحة. غير أن كل مريض يستحق تقييماً قادراً على التعرف على سبب ميكانيكي حين يكون موجوداً – وهو موجود لدى نسبة كبيرة منهم.
إعادة تأطير تقييم ارتفاع ضغط الدماغ
ينبغي أن نفهم تسمية «ارتفاع ضغط الدماغ مجهول السبب» على ما هي عليه: علامة مؤقتة تعكس حدود التقييم القياسي، لا تشخيصاً نهائياً. حين يُفحَص مسار التصريف الوريدي بعناية – من الثقبة الوداجية، عبر ممر C1، نزولاً إلى المسار العنقي الأوسط الديناميكي، ومروراً بمخرج الصدر – يمكن تحديد سبب ميكانيكي عند نسبة كبيرة من المرضى 5 20 26
انضغاط الوريد الوداجي عند الفقرة C1 ومتلازمة مخرج الصدر هما من أكثر المساهمات إغفالاً. يتقاسمان نمطاً مشتركاً للمريض، يتعايشان كثيراً، ويُنتجان صورة سريرية لا تُميَّز عن «الصورة الكلاسيكية» لارتفاع ضغط الدماغ. الحجة الميكانيكية لم تعد في باب التخمين: عمل أهن التشريحي يوثّق تضيق الوريد الوداجي الباطن عند مخرج الصدر لدى ثلاثة من كل أربعة مرضى بمتلازمة مخرج الصدر العصبية 26 وحالة شَهْوالة تُظهر التدفق العكسي إلى المنظومة الوريدية للدماغ في تصوير أوردة في الزمن الحقيقي 25 وأربعون عاماً من الأدلة الجراحية – من راسكين إلى تشا – توثّق أن إزالة الضغط عن مخرج الصدر تُخفّف الصداع الناتج عنه 27 28 التعرف على هؤلاء المرضى يستلزم استعداداً للنظر إلى ما وراء الجمجمة وتصوير مسار التصريف الوريدي بشكل ديناميكي. وعلاجهم يستلزم خبرة تجمع جراحة الأعصاب وجراحة الأوعية الدموية والإجراءات العصبية التداخلية – وهو بالضبط النهج المتعدد التخصصات الذي أُسست عليه عيادتنا.
إذا قيل لك إن لديك ارتفاع ضغط الدماغ، وأعراضك لا تتحسن، ولم يُصوَّر أحدٌ أوردتك الوداجية أو مخرج صدرك بعدُ – فهذا حديث يستحق أن يُبدأ.
انظر أيضاً
المراجع
- Friedman DI, Liu GT, Digre KB. Revised diagnostic criteria for the pseudotumor cerebri syndrome in adults and children. Neurology. 2013;81(13):1159–1165. doi:10.1212/WNL.0b013e3182a55f17[↩][↩]
- Markey KA, Mollan SP, Jensen RH, Sinclair AJ. Understanding idiopathic intracranial hypertension: mechanisms, management, and future directions. Lancet Neurol. 2016;15(1):78–91. doi:10.1016/S1474-4422(15)00298-7[↩][↩]
- Mollan SP, Davies B, Silver NC, et al. Idiopathic intracranial hypertension: consensus guidelines on management. J Neurol Neurosurg Psychiatry. 2018;89(10):1088–1100. doi:10.1136/jnnp-2017-317440[↩][↩][↩][↩]
- Wall M, Kupersmith MJ, Kieburtz KD, et al. The Idiopathic Intracranial Hypertension Treatment Trial: clinical profile at baseline. JAMA Neurol. 2014;71(6):693–701. doi:10.1001/jamaneurol.2014.133[↩]
- Fargen KM, Midtlien JP, Margraf CR, Hui FK. Idiopathic intracranial hypertension pathogenesis: The jugular hypothesis. Interv Neuroradiol. 2024 Aug 8:15910199241270660. doi:10.1177/15910199241270660[↩][↩][↩][↩][↩][↩][↩][↩][↩]
- Townsend RK, Fargen KM. Intracranial venous hypertension and venous sinus stenting in the modern management of idiopathic intracranial hypertension. Life (Basel). 2021;11(6):508. doi:10.3390/life11060508[↩]
- Bono F, Messina D, Giliberto C, et al. Bilateral transverse sinus stenosis predicts IIH without papilledema in patients with migraine. Neurology. 2006;67(3):419–423. doi:10.1212/01.wnl.0000227892.67354.85[↩]
- Mollan SP, Aguiar M, Evison F, Frew E, Sinclair AJ. The expanding burden of idiopathic intracranial hypertension. Eye (Lond). 2019;33(3):478–485. doi:10.1038/s41433-018-0238-5[↩][↩]
- Corbett JJ, Digre K. Idiopathic intracranial hypertension: an answer to “the chicken or the egg?” Neurology. 2002;58(1):5–6. doi:10.1212/wnl.58.1.5[↩]
- King JO, Mitchell PJ, Thomson KR, Tress BM. Manometry combined with cervical puncture in idiopathic intracranial hypertension. Neurology. 2002;58(1):26–30. doi:10.1212/wnl.58.1.26[↩]
- Scoffings DJ, Pickard JD, Higgins JN. Resolution of transverse sinus stenoses immediately after CSF withdrawal in idiopathic intracranial hypertension. J Neurol Neurosurg Psychiatry. 2007;78(8):911–912. doi:10.1136/jnnp.2006.111765[↩]
- Bono F, Giliberto C, Mastrandrea C, Cristiano D, Lavano A, Fera F, Quattrone A. Transverse sinus stenoses persist after normalization of the CSF pressure in IIH. Neurology. 2005;65(7):1090–1093. doi:10.1212/01.wnl.0000178889.63571.e5[↩]
- De Simone R, Ranieri A, Montella S, Bilo L, Cautiero F. The role of dural sinus stenosis in idiopathic intracranial hypertension pathogenesis: the self-limiting venous collapse feedback-loop model. Panminerva Med. 2014;56(3):201–209.[↩]
- Lim J, Monteiro A, Kuo CC, Jacoby WT, Cappuzzo JM, Becker AB, Davies JM, Snyder KV, Levy EI, Siddiqui AH. Stenting for Venous Sinus Stenosis in Patients With Idiopathic Intracranial Hypertension: An Updated Systematic Review and Meta-Analysis of the Literature. Neurosurgery. 2024;94(4):648–656. doi:10.1227/neu.0000000000002718[↩]
- Ahmed RM, Wilkinson M, Parker GD, Thurtell MJ, Macdonald J, McCluskey PJ, Allan R, Dunne V, Hanlon M, Owler BK, Halmagyi GM. Transverse Sinus Stenting for Idiopathic Intracranial Hypertension: A Review of 52 Patients and of Model Predictions. AJNR Am J Neuroradiol. 2011;32(8):1408–1414. doi:10.3174/ajnr.A2575[↩]
- Mejia-Vergara AJ, Sultan W, Kostas A, Mulholland CB, Sadun A. Styloidogenic Jugular Venous Compression Syndrome with Papilloedema: Case Report and Review of the Literature. Neuroophthalmology. 2021;46(1):54–58. doi:10.1080/01658107.2021.1887288[↩][↩][↩]
- Dashti SR, Nakaji P, Hu YC, et al. Styloidogenic jugular venous compression syndrome: diagnosis and treatment: case report. Neurosurgery. 2012;70(3):E795 – E799. doi:10.1227/NEU.0b013e3182333859[↩][↩]
- Pokeerbux MR, Delmaire C, Morell-Dubois S, Demondion X, Lambert M. Styloidogenic compression of the internal jugular vein, a new venous entrapment syndrome? Vasc Med. 2020;25(4):378–380. doi:10.1177/1358863X20902842[↩][↩]
- Scerrati A, Norri N, Mongardi L, et al. Styloidogenic-cervical spondylotic internal jugular venous compression, a vascular disease related to several clinical neurological manifestations: diagnosis and treatment – a comprehensive literature review. Ann Transl Med. 2021;9(8):718. doi:10.21037/atm-20-7698[↩][↩]
- Zhou D, Meng R, Zhang X, et al. Intracranial hypertension induced by internal jugular vein stenosis can be resolved by stenting. Eur J Neurol. 2018;25(2):365-e13. doi:10.1111/ene.13512[↩][↩][↩][↩]
- Holmlund P, Johansson E, Qvarlander S, Wåhlin A, Ambarki K, Koskinen LO, Malm J, Eklund A. Human jugular vein collapse in the upright posture: implications for postural intracranial pressure regulation. Fluids Barriers CNS. 2017;14:17. doi:10.1186/s12987-017-0065-2[↩][↩]
- San Millán Ruíz D, Gailloud P, Rüfenacht DA, Delavelle J, Henry F, Fasel JH. The craniocervical venous system in relation to cerebral venous drainage. AJNR Am J Neuroradiol. 2002;23(9):1500–1508.[↩]
- Gisolf J, van Lieshout JJ, van Heusden K, Pott F, Stok WJ, Karemaker JM. Human cerebral venous outflow pathway depends on posture and central venous pressure. J Physiol. 2004;560(Pt 1):317–327. doi:10.1113/jphysiol.2004.070409[↩]
- Marini TJ, Chughtai K, Nuffer Z, Hobbs SK, Kaproth-Joslin K. Blood finds a way: pictorial review of thoracic collateral vessels. Insights Imaging. 2019;10(1):63. doi:10.1186/s13244-019-0753-3[↩][↩]
- Chahwala V, Tashiro J, Li X, Baqai A, Rey J, Robinson HR. Venous Thoracic Outlet Syndrome as a Cause of Intractable Migraines. Ann Vasc Surg. 2017;39:285.e5–285.e8. doi:10.1016/j.avsg.2016.05.109[↩][↩][↩]
- Ahn SS, Miller TJ, Chen SW, Chen JF. Internal jugular vein stenosis is common in patients presenting with neurogenic thoracic outlet syndrome. Ann Vasc Surg. 2014;28(4):946–950. doi:10.1016/j.avsg.2013.12.009[↩][↩][↩][↩][↩]
- Raskin NH, Howard MW, Ehrenfeld WK. Headache as the leading symptom of the thoracic outlet syndrome. Headache. 1985;25(4):208–210. doi:10.1111/j.1526-4610.1985.hed2504208.x[↩][↩][↩][↩]
- Cha YH, Randall L, Weber J, Ahn S. Treatment of thoracic outlet syndrome to relieve chronic migraine. Clin Anat. 2025;38(3):314–323. doi:10.1002/ca.24242[↩][↩][↩][↩][↩]
- Midtlien JP, Curry BP, Chang E, et al. Characterizing a new clinical phenotype: the co-existence of cerebral venous outflow and connective tissue disorders. Front Neurol. 2023;14:1305972. doi:10.3389/fneur.2023.1305972[↩]
- Manupipatpong S, Primiani CT, Fargen KM, et al. Jugular venous narrowing and spontaneous spinal cerebrospinal fluid leaks: A case – control study exploring association and proposed mechanism. Interv Neuroradiol. 2024;30(6):812–818. doi:10.1177/15910199241287417[↩]
